Шановні семикласники!!!
Працюємо дистанційно.
19 травня 2020
Узагальнення
знань з теми: «Кисень.Вода». Контрольна робота
Перейти за посиланням і
виконати роботу доступ відкрито з
12
год до 14.00 год
19 травня
!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
Всі заборговані завдання приймаю
до 20.00год. 24 травня!!!👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀
Шановні семикласники!!!
Працюємо дистанційно. Всі завдання ОБОВ’ЯЗКОВІ до виконання!!!
Використовуємо підручник Попель П.
(електронний варіант додається)
Виконані завдання
надсилати
до 9 :00 год. 19 травня 2020 p.
1. !!!!! Опрацювати §22 підручник Буринська Н.М 7 клас, або
§31 підручник Попель П.
У робочому зошиті записуємо
12 травня
Тема. Проблема
чистої води. Охорона водойм від забруднення.
Очищення води
на водоочисних станціях та в домашніх умовах.
1. Складіть схеми:
·
Основні забруднювачі води.
·
Способи очищення води.
2.Вкажіть способи очищення питної води від забруднень
піском
3. Вкажіть способи очищення питної води від мікрооргінізмів
👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀
Шановні семикласники!!!
Працюємо дистанційно. Всі завдання ОБОВ’ЯЗКОВІ до виконання!!!
Використовуємо підручник Попель П. (електронний варіант додається)
Виконані завдання
надсилати
до 9:00 год. 12 травня 2020 p.
1.Перевірка
домашнього завдання.
Виконати
тести за посиланням https://vseosvita.ua/test/start/nzw472
2.Опрацювати § 30 підручник Попель П. Зробити
конспект
Переглянути урок можна за посиланням:
Що таке кислотні дощі? https://www.youtube.com/watch?v=urJZkYxTeLY
Виконати завдання
1. Назвіть найважливіші ланки колообігу води в
природі.
2. Чому більшість хімічних заводів розміщено
поблизу річок?
3. Надайте кілька пропозицій з економії води у
побуті.
4. Перетворіть схеми реакцій, які відбуваються
при випалюванні металічних руд на хімічні рівняння:
а) ZnS + O 2
→ ZnO + SO2;
б) MoS2
+ O2 → MoO3
+ SO2.
5. Виведіть формулу оксиду Нітрогену, який
взаємодіє з водою з утворенням:
А) нітритної кислоти HNО2;
Б) нітратної кислоти HNО3.
6. Обчисліть масу сульфур(ІV) оксиду, в якому
масова частка Сульфуру становить 6 %.
(Виконуємо роботу, варіант відповідає вашому робочому місці в кабінеті хімії.
Перший варіант від вікна.).
👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀👀Шановні семикласники!!!
Працюємо дистанційно. Всі завдання ОБОВ’ЯЗКОВІ до виконання!!!
Використовуємо підручник Буринська Н.М
Попель П. (електронний варіант додається)
Виконані завдання надсилати до 9 :00 год. 5 травня 2020 p.
1.Опрацювати §21 підручник Буринська Н.М
або § 28,29 підручник Попель П.
2. Переглянути
урок можна за посиланням: https://www.youtube.com/watch?v=Iv7m773LUU0&fbclid=IwAR2M6nGnW7zxMHRdsgLgcpAfNhE2hSo21t9Pd7xukI9UQ8Pa9u6-xSck3cY
3. У
робочому зошиті зробити конспект (зразок нижче), завдання з конспекту виконати
4.
Оформити лабораторний дослід 10.
Випробування водних розчинів кислот і лугів індикаторами
РОБОТИ НАДСИЛАТИ ВЧАСНО
УСПІХІВ!!!!
_____________________________________________________________________
Шановні семикласники!!!
Працюємо дистанційно.
Всі завдання обов’язкові до
виконання!!!
Використовуємо підручник Буринська Н.М
Попель П. (електронний варіант додається)
Виконані завдання надсилати до
9.00 год. 28 квітня 2020 p.
1. Повторити §19.20 підручник Буринська Н.М
§
26,27 підручник Попель П.
2. Виконати тести за посиланням:
!!! обов’язково повторити алгоритм
розв’язування задач
Час обмежений – 40хв, спроба лише
одна. Будьте уважні!!
3. Переглянути
відео: https://www.youtube.com/watch?v=So2mPmpXn0w&fbclid=IwAR3P9M-KLhoCkQi1082OmiC41Gl6S5FVIH9K_xIlyQgFJ-f62QVf97ZQfig
У робочому зошиті записуємо
21 квітня
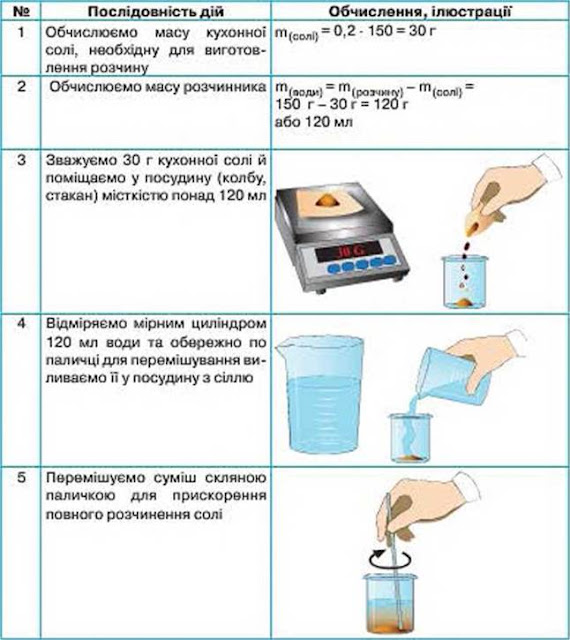
Тема. Виготовлення розчину.
Записати
у зошит послідовність дій виготовлення розчинів
Перейти за посиланням:
Виконуємо все згідно
інструкції. Записуємо в зошит.
Надсилаємо мені___________________________________________________
Шановні семикласники!!!
Працюємо дистанційно. Всі завдання
обов’язкові до виконання!!!
Використовуємо підручник Буринська Н.М
Попель П. (електронний варіант додається)
Виконані завдання
надсилати до
9.00 год. 21 квітня 2020 p.
1. Виконати тести за посиланням:
Час обмежений – 40хв, спроба лише
одна. Будьте уважні!!!
2. Опрацювати §19.20 підручник
Буринська Н.М
§ 26,27 підручник Попель П.
Переглянути відео:
Масова
частка розчиненої речовини частина І
Масова частка розчиненої речовини частина ІІ
У робочому зошиті записуємо
14 квітня
Тема. Розчин і його компоненти:
розчинник, розчинена речовина. Вода — розчинник. Кількісний склад розчину.
Масова частка розчиненої речовини.
Записати у зошит основні терміни й поняття: розчинник, розчинена
речовина, масова частка розчиненої речовини.
Задача № 1
Калій хлорид масою 30 г розчинили у воді масою 120 г . Яка масова частка
калій хлориду у добутому розчині?
Задача №2.
Які масу калій гідроксиду КОН та об’єм води
необхідно взяти для приготування 200
г розчину з масовою часткою лугу 15%?
____________________________________________________________Шановні семикласники!!!
Працюємо дистанційно. Всі завдання
обов’язкові до виконання!!!
Використовуємо підручник Буринська Н.М
Попель П. (електронний варіант додається)
Виконані завдання
надсилати до
9.00 год. 14 квітня 2020 p.
На подвійних листочках записуємо:
7 квітня 2020 р.
Контрольна
робота з теми: «Кисень»
(Виконуємо роботу, варіант відповідає вашому робочому місці в кабінеті
хімії.
Перший варіант від вікна.). Завдання зберігаємо.
У робочому зошиті записуємо
7 квітня
Тема. Вода, склад молекули, поширеність у природі, фізичні властивості.
Опрацювати §18 підручник Буринська Н.М
Конспект оформити, заповнивши таблицю
Назва речовини
|
Вода
|
Будова молекули
|
|
Хімічна формула
|
|
Відносна молекулярна маса
|
|
Колір, запах, смак
|
|
Температура замерзання води
|
|
Температура кипіння води
|
|
Густина рідкої води (г/мл) за t =
4 °C
|
|
Густина льоду (менше чи більше
води)
|
|
Під час замерзання вода
розширюється чи стискається
|
|
Електропровідність
|
Читання тексту
1. Вода
— головний розчинник на Землі. Тверді
речовини краще розчиняються за підвищеної температури, а гази — за низької
температури й підвищеного тиску.
2. У
рідкому стані вода практично не стискається, у разі охолодження від +4 до 0 °С
розширюється. Найбільшу густину (1 г/см3) вода має за
температури +4 °С. Лід має більший об’єм (у замерзлому стані розширюється на
1/11 від свого об’єму), ніж рідка вода, тому в нього менша густина, ніж у води
(0,9 г/см3). Завдяки цьому, а також малій теплопровідності шар льоду
захищає глибокі водойми від промерзання до дна, що забезпечує існування в них
живих організмів.
4. Вода
має високу теплоємність. Охолодивши 1 м3 води на 1 °С, можна
нагріти 1000 м3 повітря на 3 °С, що зумовлює досить повільну
зміну температури океанів і регуляцію температури на земній поверхні. Цим
пояснюють той факт, що клімат на островах більш помірний, ніж на материках.
5. У
води висока теплота пароутворення. Після купання влітку нам не жарко, поки
вода випаровується з поверхні нашого тіла.
____________________________________________________________________
Шановні семикласники!!!
Працюємо дистанційно. Всі завдання
обов’язкові до виконання!!!
Використовуємо підручник Буринська Н.М
Виконані
завдання надсилати до
9.00
год. 7
квітня 2020 p.
Конспектуємо у
зошит основні терміни і відповіді на запитання.
31 березня 2020
Тема.
Колообіг Оксигену в природі. Озон. Проблема
чистого повітря. Застосування та біологічна роль кисню. Узагальнення знань з теми: «Кисень»
РЕКОМЕДУЮ використовувати підручник ПОПЕЛЬ
П. 7 клас
!!!!!
Опрацювати §24 підручник Попель П. ( Повторити §18-22)
§16 підручник Буринська Н.М 7 клас. ( Повторити §
12-16)
Конспектуємо у зошит основні терміни і відповіді на
запитання:
Пройти
тестування на Всеосвіта (вказавши ім’я
та прізвище) за запрошенням
код: mqv173
Виконати
завдання 6 квітня з 19.00 до 19.40.
Час
виконання обмежений – 40 хв, слова вставляти з МАЛОЇ літери, якщо інше не
вказано. Фото результату надішліть мені на Viber або електронну пошту.
_________________________________________________________________________________
Шановні семикласники!!!
Працюємо дистанційно. Всі завдання
обов’язкові до виконання!!!
Використовуємо підручник Буринська
Н.М
Виконані завдання
надсилати до
9.00 год. 31 березня 2020
p.
Переглянути
урок можна за посиланням:
Перевірити
знання :
17 березня 2020
Тема. Поняття про оксиди, окиснення (
горіння, повільне окиснення, дихання).
Умови виникнення та припинення горіння .
Тема. Взаємодія кисню з простими і
складними речовинами
!!!!! Опрацювати §15
підручник Буринська Н.М 7 клас.
§21,22 підручник Попель П.
Конспектуємо у зошит основні терміни і
відповіді на запитання
●
оцінити здатність кисню
вступати в реакції з простими і деякими складними речовинами; оксиди
●
порівняти процеси
горіння і окиснення;
●
з’ясувати умови,
необхідні для горіння речовин, а також для припинення цього процесу.
Виконати завдання:
1.Чим різняться реакції сполучення і розкладу?
2. Виберіть серед наведених формул ті, що відповідають
оксидам: O2, NaOH, H2O, HCl, I2O5,
BaO.
3.Встановіть відповідність: Формула оксиду Назва оксиду 1) FeO; а) ферум(ІІІ) оксид;
2) Fe2O3; б) ферум(ІІ, ІІІ) оксид; 3)
Fe3O4; в) ферум(ІІ) оксид.
4.Дайте хімічні назви оксидам із такими формулами: NO, Ti2O3,
Cu2O, Cl2O7, V2O5, CrO3.
Зважте на те, що елементи, які утворюють ці оксиди, мають змінну валентність.
5.Запишіть формули плюмбум(IV) оксиду, хром(III) оксиду,
хлор(І) оксиду, осмій(VIII) оксиду.
6.Допишіть формули простих речовин у схемах реакцій і
складіть хімічні рівняння:
7.Назвіть усі можливі значення індексу n у загальній формулі
оксидів ЕmОn, якщо:
а) m = 1; б) m = 2.
8.Обчисліть масову частку Оксигену в гідроген пероксиді.
9.Яке явище називають горінням? Назвіть умови, необхідні для
перебігу цього процесу. 166.Чи можна вважати, що в електролампочці відбувається
реакція горіння металевої (вольфрамової) спіралі? Чому?
10.Якими способами можна загасити полум’я?
11.Зіставте значення термінів «горіння», «окиснення» і
скажіть, який із них є більш загальним. Відповідь поясніть.
13.Перетворіть схеми
реакцій на хімічні рівняння:
а) FeO + O 2 → Fe 2O3; SiH 4 + O2 → SiO 2 + H2O;
б) Mn 2O3 + O2 → MnO 2; NH 3 + O2 → N 2 + H2O.
15.Складіть рівняння реакцій горіння на повітрі ацетону (СН3)2СО
та етеру (С2Н5)2О.
16.У трьох посудинах без етикеток містяться повітря, кисень
і вуглекислий газ. Як можна визначити вміст кожної посудини?